Provigil: Uyanıklık Tedavisi (Tam Reçete Bilgisi)
Marka Adı: Provigil
Genel Adı: Modafinil
İçindekiler:
Açıklama
Farmakoloji
Klinik İzler
Göstergeler ve kullanımları
Kontrendikasyonlar
Uyarılar
Önlemler
Ters tepkiler
Uyuşturucu Kullanımı ve Bağımlılığı
Doz Aşımı
Dozaj ve Uygulama
Nasıl tedarik edildi
Provigil (modafinil) hasta bilgi sayfası (Sade ingilizce)
Açıklama
Provigil (modafinil) oral uygulama için uyanıklığı destekleyen bir ajandır. Modafinil rasemik bir bileşiktir. Modafinil'in kimyasal adı 2 - [(difenilmetil) sülfinil] asetamiddir. Moleküler formül C15H15N02S'dir ve moleküler ağırlık 273.35'tir.
Kimyasal yapı:
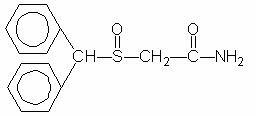
Modafinil, su ve sikloheksan içinde pratik olarak çözünmeyen beyaz ila kirli beyaz bir kristal tozdur. Metanol ve asetonda az çözünür. Provigil tabletleri 100 mg veya 200 mg modafinil ve aşağıdaki aktif olmayan bileşenleri içerir: laktoz, mikrokristalin selüloz, önceden jelatinize edilmiş nişasta, kroskarmeloz sodyum, povidon ve magnezyum stearatla.
üst
Klinik Farmakoloji
Eylem Mekanizması ve Farmakolojisi
Modafinil'in uyanıklığı teşvik ettiği kesin mekanizmalar bilinmemektedir. Modafinil, farmakolojik profil sempatomimetik aminlerinki ile aynı olmasa da, amfetamin ve metilfenidat gibi sempatomimetik ajanlara benzer uyanıklık verici etkilere sahiptir.
Modafinil, norepinefrin, serotonin, dopamin, GABA, adenosin, histamin-3, melatonin ve benzodiazepinler için reseptörlerle zayıf veya ihmal edilebilir etkileşimlere sahiptir. Modafinil ayrıca MAO-B veya fosfodiesterazlar II-V'nin aktivitelerini inhibe etmez.
Modafinil kaynaklı uyanıklık, Î ± 1-adrenerjik reseptör antagonisti prazosin ile zayıflatılabilir; bununla birlikte modafinil, sıçan vas deferens preparatı gibi Î ± -adrenerjik agonistlere yanıt verdiği bilinen diğer in vitro test sistemlerinde aktif değildir.
Modafinil, doğrudan veya dolaylı etkili bir dopamin reseptör agonisti değildir. Bununla birlikte, in vitro olarak, modafinil dopamin taşıyıcısına bağlanır ve dopamin geri alımını inhibe eder. Bu aktivite, hayvanların bazı beyin bölgelerinde hücre içi dopamin düzeylerinde artış ile in vivo olarak ilişkilendirilmiştir. Dopamin taşıyıcı (DAT) içermeyen genetik olarak tasarlanmış farelerde modafinil, uyanıklığı arttırıcı aktiviteden yoksundu ve bu aktivitenin DAT bağımlı olduğunu düşündürdü. Bununla birlikte, modafinilin amfetamininkinden farklı olarak uyandırıcı etkileri, sıçanlarda dopamin reseptör antagonisti haloperidol tarafından antagonize edilmemiştir. Ek olarak, bir dopamin sentez inhibitörü olan alfa-metil-p-tirosin, amfetaminin etkisini bloke eder, ancak modafinil tarafından indüklenen lokomotor aktivitesini bloke etmez.
Kedide, uyanıklığı artıran metilfenidat ve amfetamin dozları, beyin boyunca nöronal aktivasyonu arttırdı. Modafinil, eşdeğer bir uyanıklığı artıran dozda, beynin daha ayrık bölgelerinde seçici ve belirgin bir şekilde nöronal aktivasyonu arttırdı. Kedilerde bu bulgunun insanlarda modafinilin etkileri ile ilişkisi bilinmemektedir.
Uyanıklığı artırıcı etkilerine ve hayvanlarda lokomotor aktivitesini arttırma yeteneğine ek olarak modafinil, psikoaktif ve öforik etkiler, ruh halindeki değişiklikler, algı, düşünme ve diğer CNS uyarıcılarına özgü duygular insanlarda. Modafinil, daha önce kendi kendini yöneten kokain için eğitilmiş maymunlarda kendi kendine uygulama ile kanıtlandığı gibi, güçlendirici özelliklere sahiptir. Modafinil ayrıca uyarıcı benzeri olarak kısmen ayırt edildi.
Modafinilin optik enantiyomerleri hayvanlarda benzer farmakolojik etkilere sahiptir. Modafinil, modafinil asit ve modafinil sülfonun iki ana metaboliti, modafinil'in CNS aktive edici özelliklerine katkıda bulunmaz gibi görünmektedir.
Farmakokinetik
Modafinil, enantiomerleri farklı farmakokinetiğe sahip olan rasemik bir bileşiktir (örneğin, l-izomerin yarı ömrü, yetişkin insanlarda d-izomerin yaklaşık üç katıdır). Enantiyomerler birbirine geçmez. Kararlı durumda, l-izomere toplam maruz kalma, d-izomere göre yaklaşık üç kat daha fazladır. Çukur konsantrasyonu (Cminss) günde bir kez dozlamadan sonra dolaşımdaki modafinilin l-izomerinin% 90'ı ve d-izomerinin% 10'undan oluşur. Modafinil'in çoklu dozlardan sonra etkili eliminasyon yarılanma ömrü yaklaşık 15 saattir. Modafinil enantiomerleri, sağlıklı gönüllülerde günde bir kez 200-600 mg / gün çoklu dozlama üzerine lineer kinetik sergiler. Toplam modafinil ve l - (-) - modafinil'in görünür kararlı durumlarına 2-4 günlük dozlamadan sonra ulaşılır.
emme
Provigil tabletlerin emilimi hızlıdır, pik plazma konsantrasyonları 2-4 saatte gerçekleşir. Provigil tabletlerinin biyoyararlanımı yaklaşık olarak sulu bir süspansiyonun biyoyararlanımıdır. İntravenöz uygulamayı engelleyen modafinilin sulu çözünmezliği (<1 mg / mL) nedeniyle mutlak oral biyoyararlanım belirlenmedi. Yiyeceklerin genel Provigil biyoyararlanımı üzerinde hiçbir etkisi yoktur; ancak emilimi (tmaksimum), yiyecekle birlikte alındığında yaklaşık bir saat geciktirilebilir.
dağıtım
Modafinil, vücut kütlesinde, toplam vücut suyu hacminden (0.6 L / kg) daha büyük bir dağılım hacmi (~ 0.9 L / kg) ile iyi bir şekilde dağılır. İnsan plazmasında, in vitro olarak, modafinil plazma proteinine orta derecede bağlanır (esas olarak albümine ~% 60). 200 mg / gün dozlardan sonra kararlı halde elde edilen serum konsantrasyonlarında, modafinil varfarin, diazepam veya propranololün protein bağlanmasında yer değiştirme göstermez. Çok daha büyük konsantrasyonlarda bile (1000 uM; > C'nin 25 katımaksimum 400 mg / gün kararlı durumda 40 uM), modafinilin varfarin bağlanması üzerinde bir etkisi yoktur. > 500 uM konsantrasyonlardaki modafinil asit, varfarin bağlanma derecesini azaltır, ancak bu konsantrasyonlar, terapötik olarak elde edilen konsantrasyonların> 35 katıdır.
Metabolizma ve Eliminasyon
Ana eliminasyon yolu, metabolitlerin (daha sonra% 90), öncelikle karaciğer tarafından, daha sonra metabolitlerin renal eliminasyonu ile ilgilidir. İdrar alkalinizasyonunun modafinilin ortadan kaldırılması üzerinde hiçbir etkisi yoktur.
Metabolizma hidrolitik deamidasyon, S-oksidasyon, aromatik halka hidroksilasyon ve glukuronid konjügasyonu ile ortaya çıkar. Uygulanan bir dozun% 10'undan azı ana bileşik olarak atılır. Radyoaktif işaretli modafinil kullanan bir klinik çalışmada, uygulanan radyoaktivitenin toplam% 81'i dozdan sonraki 11 gün içinde, ağırlıklı olarak idrarda (% 80'e karşı) Dışkıda% 1.0). İlacın idrardaki en büyük kısmı modafinil asitti, ancak en az altı başka metabolit daha düşük konsantrasyonlarda mevcuttu. Plazmada sadece iki metabolit, yani modafinil asit ve modafinil sülfonda kayda değer konsantrasyonlara ulaşır. Klinik öncesi modellerde modafinil asit, modafinil sülfon, 2 - [(difenilmetil) sülfonil] asetik asit ve 4-hidroksi modafinil aktif değildir veya modafinil'in uyarılma etkilerine aracılık ettiği görülmemiştir.
Yetişkinlerde, birkaç haftalık dozlamadan sonra bazen modafinil çukur seviyelerinde azalma gözlenmiştir. oto-indüksiyon, ancak azalmaların büyüklüğü ve oluşumlarının tutarsızlığı, klinik önemlerinin minimaldir. 40 saatlik uzun eliminasyon yarılanma ömrü nedeniyle çoklu dozlardan sonra modafinil sülfonun önemli miktarda biriktiği gözlenmiştir. Metabolize edici enzimlerin, en önemlisi sitokrom P-450 (CYP) 3A4'ün indüksiyonu ayrıca in vitro olarak gözlemlenmiştir. İnsan hepatositlerinin birincil kültürlerinin modafinil ve in vivo ile inkübasyonunun, 400 mg / gün. (Modafinilin CYP enzim aktiviteleri üzerindeki etkileri hakkında daha fazla tartışma için bkz. ÖNLEMLER, İlaç etkileşimleri.)
İlaç-İlaç Etkileşimleri:
In vitro verilere dayanarak, modafinil kısmen hepatik sitokrom P450'nin (CYP3A4) 3A izoform alt ailesi tarafından metabolize edilir. Ek olarak, modafinil CYP2C19'u inhibe etme, CYP2C9'u baskılama ve CYP3A4, CYP2B6 ve CYP1A2'yi indükleme potansiyeline sahiptir. Modafinil ve modafinil sülfon, ilaç metabolize edici enzim CYP2C19'un geri dönüşümlü inhibitörleri olduğundan, modafinilin bu yolla büyük ölçüde yok edilen diazepam, fenitoin ve propranolol gibi ilaçlar, bunların dolaşım seviyelerini artırabilir. Bileşikler. Ek olarak, CYP2D6 enziminde eksik olan bireylerde (yani, Kafkas popülasyonunun% 7-10'u; diğer popülasyonlarda benzer veya daha düşük), trisiklik antidepresanlar ve seçici serotonin gibi CYP2D6 substratlarının seviyeleri CYP2C19 yoluyla yardımcı eliminasyon yollarına sahip geri alım inhibitörleri, modafinil. Bu ve benzeri ilaçlarla tedavi edilen hastalar için doz ayarlamaları gerekebilir (Bkz. ÖNLEMLER, İlaç etkileşimleri). Bir in vitro çalışma, armodafinilin (modafinil enantiyomerlerinden biri) bir P-glikoproteinin substratı olduğunu göstermiştir.
Modafinil'in metilfenidat ve dekstroamphetamin gibi diğer CNS aktif ilaçlarla birlikte uygulanması, her iki ilacın farmakokinetiğini önemli ölçüde değiştirmedi.
Modafinil 400 mg'ın kronik uygulanmasının iki CYP3A4'e sistemik maruziyeti azalttığı bulundu. oral uygulamadan sonra CYP3A4'ün olduğunu gösteren substratlar, etinil estradiol ve triazolam neden oldu. Modafinilin kronik uygulaması CYP3A4 substratlarının eliminasyonunu artırabilir. Bu ve benzeri ilaçlarla tedavi edilen hastalar için doz ayarlamaları gerekebilir (Bkz. ÖNLEMLER, İlaç etkileşimleri).
İnsan hepatositlerinde in vitro modafinil maruziyetinden sonra konsantrasyona bağlı bir CYP2C9 aktivitesinin baskılanması gözlendi modafinil ile bu enzimin substratları arasında metabolik bir etkileşim potansiyeli olduğunu düşündürmektedir (örneğin, S-varfarin, fenitoin). Bununla birlikte, sağlıklı gönüllülerde yapılan bir etkileşim çalışmasında, kronik modafinil tedavisi, varfarinin farmakokinetiği üzerinde plaseboya kıyasla anlamlı bir etki göstermemiştir. (Görmek ÖNLEMLER, İlaç Etkileşimleri, Diğer İlaçlar, Warfarin).
Özel Nüfuslar
Cinsiyet Etkisi:
Modafinil'in farmakokinetiği cinsiyetten etkilenmez.
Yaş Etkisi:
Modafinil'in oral klerensinde (CL / F) hafif bir azalma (~% 20), 12 mg'da 200 mg'da tek bir doz çalışmasında gözlenmiştir. yaş ortalaması 63 (dağılım 53-72) olan, ancak bu değişikliğin klinik olarak muhtemel olmadığı düşünülüyor önemli. Ortalama 82 yaş (dağılım 67-87 yıl) olan 12 hastada yapılan çoklu doz çalışmasında (300 mg / gün) ortalama plazmada modafinil seviyeleri, eşleştirilmiş gençlerde tarihsel olarak elde edilenlerin yaklaşık iki katıdır konular. Hastaların çoğunun bulunduğu çoklu eşlik eden ilaçların potansiyel etkileri nedeniyle tedavi edildiğinde, modafinil farmakokinetiğindeki belirgin fark sadece yaşlanma. Bununla birlikte, sonuçlar yaşlılarda modafinil klerensinin azaltılabileceğini düşündürmektedir (Bkz. Dozaj ve Uygulama).
Yarış Etkisi:
Irkın modafinil farmakokinetiği üzerindeki etkisi araştırılmamıştır.
Böbrek yetmezliği:
Tek doz 200 mg modafinil çalışmasında, şiddetli kronik böbrek yetmezliği (kreatinin klerensi mL ‰ ¤ 20 mL / dak) modafinil'in farmakokinetiğini önemli ölçüde etkiler, ancak modafinil aside (aktif olmayan bir metabolit) maruziyet artmıştır. 9 kat (Bkz. ÖNLEMLER).
Karaciğer yetmezliği:
Karaciğer sirozu olan hastalarda (6 erkek ve 3 kadın) farmakokinetik ve metabolizma incelenmiştir. Üç hastada evre B veya B + siroz vardı (Çocuk kriterlerine göre) ve 6 hastada evre C veya C + siroz vardı. Klinik olarak 9 hastanın 8'inde ikterik ve hepsinde asit vardı. Bu hastalarda, modafinil'in oral klerensi yaklaşık% 60 azalmış ve stabil durum konsantrasyonu normal hastalara göre iki katına çıkarılmıştır. Şiddetli karaciğer yetmezliği olan hastalarda Provigil dozu azaltılmalıdır (Bkz. ÖNLEMLER ve Dozaj ve Uygulama).
üst
Klinik İzler
Provigil'in aşırı uykuyu azaltmada etkinliği aşağıdaki uykuda belirlenmiştir. bozuklukları: narkolepsi, obstrüktif uyku apnesi / hipopne sendromu (OSAHS) ve vardiyalı çalışma uyku bozukluğu (SWSD).
narkolepsi
Provigil'in narkolepsi ile ilişkili aşırı uykululuk oranını (ES) azaltmada etkinliği ABD'de 9 haftada iki, çok merkezli, plasebo kontrollü, iki doz (günde 200 mg ve günde 400 mg) paralel grup, ICD-9 ve Amerikan Uyku Bozuklukları Birliği narkolepsi kriterleri (Amerikan Psikiyatri Birliği ile de uyumludur) DSM-IV kriterleri). Bu kriterler arasında ya 1) en az üç ay boyunca neredeyse her gün meydana gelen tekrarlayan gündüz uykuları veya uykuya dalmalar, artı yoğun duygu (katapleksi) ile ilişkili ani iki taraflı postural kas tonusu kaybı veya 2) aşırı uykululuk şikayeti veya ilişkili özellikler ile ani kas güçsüzlüğü: uyku felci, hipnagojik halüsinasyonlar, otomatik davranışlar, ana uyku bozukluğu bölüm; ve aşağıdakilerden birini gösteren polisomnografi: uyku gecikmesi 10 dakikadan az veya hızlı göz hareketi (REM) uyku gecikmesi 20 dakikadan az. Ek olarak, bu çalışmalara giriş için tüm hastaların objektif olarak aşırı gündüz uykululuk hali olan Çoklu Uyku'yı belgelemeleri gerekiyordu. İki veya daha fazla uyku başlangıçlı REM periyodu olan ve klinik olarak anlamlı başka aktif tıbbi veya psikiyatrik olmayan Gecikme Testi (MSLT) bozukluk. MSLT, hastanın uyarıcı olmadan uykuya dalma yeteneğinin nesnel bir gündüz polisomnografik değerlendirmesi ortam, gece sonra 2 saatlik aralıklarla 4 test seansı boyunca ortalama uyku başlangıcındaki gecikmeyi (dakika cinsinden) ölçer polisomnografi. Her test oturumu için denekten sessizce uzanması ve uyumaya çalışması söylendi. Her test oturumu, hiç uyku oluşmadığı takdirde 20 dakika sonra veya uyku başladıktan 15 dakika sonra sonlandırıldı.
Her iki çalışmada da, etkinliğin birincil ölçüleri 1) Uyanıklığın Bakımı Testi ile değerlendirildiği üzere uyku gecikmesi idi. (MWT) ve 2) Klinik Global Değişim İzlenimi (CGI-C) ile ölçülen hastanın genel hastalık durumundaki değişiklik. Başarılı bir deneme için, her iki tedbirin de önemli ölçüde iyileşme göstermesi gerekiyordu.
MWT, gece polisomnografisini takiben 2 saatlik aralıklarla ortalama 4 test seansı boyunca uyku başlangıcındaki gecikmeyi (dakika olarak) ölçer. Her test oturumu için denekten olağanüstü önlemler almadan uyanık kalmaya çalışması istendi. Her test oturumu, hiç uyku oluşmadığı takdirde 20 dakika sonra veya uyku başladıktan 10 dakika sonra sonlandırıldı. CGI-C, No Change merkezli ve Çok Daha Kötü'den Çok Geliştirilmiş'e kadar değişen 7 noktalı bir ölçektir. Hastalar, başlangıçtaki şiddetlerinin ölçüsü dışında hastalar hakkında herhangi bir veriye erişimi olmayan değerlendiriciler tarafından derecelendirildi. Değerlendiricilere hastaları derecelendirirken uygulayacakları kriterler hakkında özel bir rehberlik verilmemiştir.
Diğer etki değerlendirmeleri arasında Çoklu Uyku Gecikme Testi (MSLT), Epworth Uykululuk Ölçeği (ESS; günlük durumlarda uykululuk derecesini değerlendirmek için tasarlanmış bir dizi soru) Steer Clear Performance Test (SCPT; hastanın simüle edilmiş bir sürüş durumunda engellere çarpmama yeteneğinin bilgisayar tabanlı bir değerlendirmesi), standart gece polisomnografisi ve hastanın günlük uyku günlüğü. Hastalar ayrıca valide edilmiş SF-36 sağlık anketini içeren Narkolepside Yaşam Kalitesi (QOLIN) ölçeği ile değerlendirildi.
Her iki çalışma, plaseboya kıyasla hem 200 mg hem de 400 mg dozlar için gündüz aşırı uykuluğun objektif ve subjektif ölçümlerinde iyileşme gösterdi. Her iki Provigil dozu ile tedavi edilen hastalar, MWT'de uyanık kalmak için istatistiksel olarak anlamlı derecede gelişmiş bir yetenek gösterdi (tüm p değerleri <0.001) 3., 6., 9. haftalar ve son ziyaret, plasebo ile karşılaştırıldığında ve CGI-C ölçeğinde (tüm p değerleri) istatistiksel olarak anlamlı derecede daha büyük bir küresel iyileşme <0.05).
2 kontrollü çalışma için başlangıçta MWT üzerindeki ortalama uyku gecikmeleri (dakika olarak), son ziyarette MWT üzerindeki taban çizgisinden ortalama değişim ile birlikte aşağıdaki Tablo 1'de gösterilmektedir.
İki klinik çalışmada CGI-C üzerinde herhangi bir gelişme derecesi gösteren hastaların yüzdeleri aşağıdaki Tablo 2'de gösterilmiştir.
Benzer istatistiksel olarak anlamlı tedavi ile ilgili iyileşmeler, bir hasta dahil olmak üzere narkolepsi, ESS'de gündüz uyku hali düzeyini değerlendirdi (her doz için p <0.001) plasebo).
Polisomnografi ile ölçülen gece uykusu Provigil kullanımından etkilenmedi.
Obstrüktif Uyku Apnesi / Hipopne Sendromu (OSAHS)
Provigil'in OSAHS ile ilişkili aşırı uykululuk oranının azaltılmasındaki etkinliği iki klinik çalışmada belirlenmiştir. Her iki çalışmada da, Uluslararası Uyku Bozuklukları Sınıflaması ile tanışan hastalar çalışmaya alındı. OSAHS (ICSD) kriterleri (Amerikan Psikiyatri Birliği DSM-IV ile de uyumludur) ölçüt). Bu kriterler ya 1) aşırı uyku hali veya uykusuzluk ile sık sık bozulmuş atakları içerir uyku sırasında nefes alma ve yüksek horlama, sabah baş ağrısı ve ağız kuruluğu gibi ilişkili özellikler uyanma; veya 2) aşağıdakilerden birini gösteren aşırı uyku hali veya uykusuzluk ve polisomnografi: her biri saatte 10 saniyeden fazla olan beşten fazla obstrüktif apne ve aşağıdakilerden biri veya daha fazlası: apne, bradikokardi ve arteriyel oksijen desatürasyonu ile ilişkili uykudan sık sık uyarılma apnealar. Ek olarak, bu çalışmalara giriş için, tüm hastaların gösterildiği gibi aşırı uyku hali olması gerekiyordu. sürekli pozitif hava yolu basıncı ile tedaviye rağmen, Epworth Uykululuk Ölçeğinde 10 puan ile (CPAP). CPAP kullanımının belgelenmesi ile birlikte CPAP'ın apne / hipopne ataklarını azaltmada etkili olduğuna dair kanıt gereklidir.
İlk çalışmada, 12 haftalık çok merkezli bir plasebo kontrollü çalışma, toplam 327 hasta Provigil 200 mg / gün, Provigil 400 mg / gün veya eşleşen plasebo alacak şekilde randomize edildi. Hastaların çoğunluğu (% 80),>% 70 gecede> 4 saat / gece CPAP kullanımı olarak tanımlanan CPAP ile tamamen uyumluydu. Kalan kısmı CPAP uyumluydu, CPAP kullanımı% 30 gece olarak tanımlandı. CPAP kullanımı çalışma boyunca devam etti. Birincil etkinlik ölçütleri, 1) Uyanıklığın Korunması Testi (MWT) ve 2) 12. haftada veya finalde Klinik Global Değişim İzlenimi (CGI-C) ile ölçülen hastanın genel hastalık durumundaki değişiklik ziyaret etmek. (Görmek Klinik İzler, Bu testlerin açıklaması için yukarıdaki Narkolepsi bölümü.)
Provigil ile tedavi edilen hastalar, uç noktada MWT (p <0.001) ile ölçüldüğü gibi plasebo ile tedavi edilen hastalara kıyasla uyanık kalmak [Tablo 1]. Provigil ile tedavi edilen hastalar ayrıca CGI-C ölçeği ile derecelendirildiği gibi klinik durumda istatistiksel olarak anlamlı bir iyileşme gösterdi (p <0.001) [Tablo 2]. İki doz Provigil benzer şekilde gerçekleştirildi.
4 haftalık çok merkezli plasebo kontrollü bir çalışmada ikinci çalışmada 157 hasta Provigil 400 mg / gün veya plasebo için randomize edildi. Tüm hastalar için düzenli CPAP kullanımının belgelenmesi (gecelerin% 70'inde en az 4 saat / gece) gerekliydi. Birincil sonuç ölçütü, 4. haftada ESS'deki başlangıç noktasından değişim veya son ziyaretti. Provigil ve plasebo grupları için başlangıç ESS skorları sırasıyla 14.2 ve 14.4 idi. 4. haftada, ESS, Provigil grubunda 4.6 ve plasebo grubunda 2.0 azaldı ve bu istatistiksel olarak anlamlıydı (p <0.0001).
Polisomnografi ile ölçülen gece uykusu Provigil kullanımından etkilenmedi.
Vardiyalı Çalışma Uyku Bozukluğu (SWSD)
Provigil'in SWSD ile ilişkili aşırı uyku hali için etkinliği, 12 haftalık plasebo kontrollü bir klinik çalışmada gösterilmiştir. Toplam 209 kronik SWSD hastası, 200 mg / gün Provigil veya plasebo almak üzere randomize edildi. Tüm hastalar, kronik SWSD için Uluslararası Uyku Bozuklukları Sınıflaması (ICSD-10) kriterlerini karşıladı ( Ritim Uyku Bozukluğu için DSM-IV Amerikan Psikiyatri Birliği kriterlerine uygun: Vardiyalı Çalışma ) Yazın. Bu kriterler şunları içerir: 1) ya: a) geçici olarak bir çalışma süresi (genellikle gece çalışması) ile ilişkili olan aşırı uyku hali veya uykusuzluktan kaynaklanan birincil şikayet alışılmış uyku fazı sırasında meydana gelir veya b) polisomnografi ve MSLT normal bir uyku-uyanıklık paterni kaybı gösterir (yani, bozulmuş kronobiyolojik ritmisite); ve 2) hiçbir tıbbi veya zihinsel bozukluk semptomları açıklamaz ve 3) semptomlar kriterleri karşılamaz uykusuzluk veya aşırı uyku hali üreten diğer uyku bozuklukları için (örn. zaman dilimi değişikliği [jet lag] sendromu).
Vardiyalı çalışma ile uğraşan uykululuk şikayeti olan tüm hastaların SWSD tanısı kriterlerini karşılamadığı unutulmamalıdır. Klinik çalışmaya sadece en az 3 aydır semptomatik olan hastalar dahil edildi.
Kayıtlı hastaların ayda en az 5 gece vardiyası çalışması, aşırı uyku hali gece vardiyalarının zamanı (MSLT skoru <6 dakika) ve gündüz uykusuzluğunun gündüz polisomnogramıyla belgelenmesi (PSG).
Birincil etkililik ölçütleri, 1) uyku haftası gecikmesiydi, 12. haftada simüle edilmiş gece vardiyası sırasında gerçekleştirilen Çoklu Uyku Gecikme Testi (MSLT) veya son ziyaret ve 2) 12. haftada ya da finalde Klinik Global Değişim İzlenimi (CGI-C) ile ölçüldüğü üzere hastanın genel hastalık durumundaki değişiklik ziyaret etmek. Provigil ile tedavi edilen hastalar, uyku MSLT ile ölçüldüğü gibi, plasebo ile tedavi edilen hastalara kıyasla uyku başlangıcında istatistiksel olarak anlamlı bir uzama gösterdi [Tablo 1] (p <0.05). CGI-C'deki iyileşmenin de istatistiksel olarak anlamlı olduğu gözlendi (p <0.001). (Görmek Klinik İzler, Bu testlerin açıklaması için yukarıdaki Narkolepsi bölümü.)
Polisomnografi ile ölçülen gündüz uyku Provigil kullanımından etkilenmedi.
HTML panosu
| düzensizlik | Tedbir | Provigil 200 mg * |
Provigil 400 mg * |
plasebo | |||
| * Tüm denemeler için plasebodan önemli ölçüde farklı (SWSD hariç tüm denemeler için p <0.01, p <0.05) | |||||||
| Temel | Değişiklik Taban çizgisinden |
Temel | Değişiklik Taban çizgisinden |
Temel | Şundan değiştir Temel |
||
| Narkolepsi I | MWT | 5.8 | 2.3 | 6.6 | 2.3 | 5.8 | -0.7 |
| Narkolepsi II | MWT | 6.1 | 2.2 | 5.9 | 2.0 | 6.0 | -0.7 |
| OUAHS | MWT | 13.1 | 1.6 | 13.6 | 1.5 | 13.8 | -1.1 |
| SWSD | MSLT | 2.1 | 1.7 | - | - | 2.0 | 0.3 |
| düzensizlik | Provigil 200 mg * |
Provigil 400 mg * |
plasebo |
| * Tüm denemeler için plasebodan önemli ölçüde farklı (p <0.01) | |||
| Narkolepsi I | 64% | 72% | 37% |
| Narkolepsi II | 58% | 60% | 38% |
| OUAHS | 61% | 68% | 37% |
| SWSD | 74% | - | 36% |
üst
Göstergeler ve kullanımları
Provigil, narkolepsi, obstrüktif uyku apnesi / hipopne sendromu ve vardiyalı iş uyku bozukluğu ile ilişkili aşırı uykuluğu olan yetişkin hastalarda uyanıklığı arttırdığı belirtilmektedir.
OSAHS'da Provigil, altta yatan tıkanıklık için standart tedaviye / tedavilere ek olarak endikedir. Sürekli pozitif hava yolu basıncı (CPAP) bir hasta için tercih edilen tedavi yöntemiyse, Provigil'i başlatmadan önce CPAP ile yeterli bir süre tedavi etmek için azami çaba gösterilmelidir. Provigil, CPAP ile yardımcı olarak kullanılıyorsa, CPAP uyumunun teşvik edilmesi ve periyodik olarak değerlendirilmesi gerekir.
Her durumda, altta yatan uyku bozukluk (lar) ının tanı ve tedavisine dikkat etmek son derece önemlidir. Reçete yazan kişiler, bazı hastaların aşırı uykululuklarına katkıda bulunan birden fazla uyku bozukluğuna sahip olabileceğinin farkında olmalıdır.
Modafinil'in uzun süreli kullanımdaki etkinliği (Narkolepsi klinik çalışmalarında 9 haftadan fazla ve 12 OSAHS ve SWSD klinik çalışmalarında haftalar) plasebo kontrollü olarak sistematik olarak değerlendirilmemiştir denemeler. Narkolepsi, OSAHS veya SWSD hastalarında Provigil'i uzun süre reçete etmeyi seçen doktor, bireysel hasta için uzun süreli yararlılığı periyodik olarak yeniden değerlendirmelidir.
üst
Kontrendikasyonlar
Provigil, modafinil, armodafinil veya aktif olmayan bileşenlerine karşı aşırı duyarlılığı olduğu bilinen hastalarda kontrendikedir.
üst
Uyarılar
Stevens-Johnson Sendromu dahil olmak üzere Ciddi Döküntü
Modafinil kullanımı ile ilişkili olarak yetişkinlerde ve çocuklarda hastaneye yatmayı ve tedavinin kesilmesini gerektiren ciddi döküntü bildirilmiştir.
Modafinil, herhangi bir endikasyon için çocuk hastalarda kullanım için onaylanmamıştır.
Modafinil klinik çalışmalarında, pediatrik hastalarda (yaş <17 yaş) kesilme ile sonuçlanan döküntü insidansı yaklaşık% 0.8 (1.585'de 13); bu döküntüler arasında 1 olası Stevens-Johnson Sendromu vakası (SJS) ve 1 vakada çok organlı aşırı duyarlılık reaksiyonu vardı. Olguların bir kısmı ateş ve diğer anormallikler (örn. Kusma, lökopeni) ile ilişkiliydi. Kesilme ile sonuçlanan ortalama döküntü süresi 13 gündür. Plasebo alan 380 pediatrik hastada böyle bir vaka gözlenmemiştir. Modafinil'in yetişkin klinik çalışmalarında (4.264'de 0) ciddi deri döküntüleri bildirilmemiştir.
SJS, Toksik Epidermal Nekroliz (TEN) ve İlaç Döküntüsü gibi nadir veya ciddi hayatı tehdit eden döküntü vakaları Dünya çapında pazarlama sonrası yetişkinlerde ve çocuklarda eozinofili ve Sistemik Belirtiler (DRESS) bildirilmiştir deneyim. Genellikle eksik raporlamaya bağlı olarak hafife alındığı kabul edilen modafinil kullanımı ile ilişkili TEN ve SJS'nin raporlama oranı, arka plan insidans oranını aşmaktadır. Genel popülasyondaki bu ciddi cilt reaksiyonları için arka plan insidansının tahminleri milyon kişi yılı başına 1-2 vaka arasında değişmektedir.
Modafinil ile ilişkili döküntü riskini veya şiddetini tahmin ettiği bilinen hiçbir faktör yoktur. Modafinil ile ilişkili hemen hemen tüm ciddi döküntü vakaları, tedavinin başlamasından 1 ila 5 hafta sonra ortaya çıktı. Bununla birlikte, uzun süreli tedaviden sonra (örneğin 3 ay) izole olgular bildirilmiştir. Buna göre, tedavinin süresine, döküntülerin ilk ortaya çıkmasıyla ortaya çıkan potansiyel riski tahmin etme aracı olarak güvenilemez.
Modafinil ile iyi huylu döküntüler de ortaya çıksa da, hangi döküntülerin ciddi olduğunu kanıtlayacağını güvenilir bir şekilde tahmin etmek mümkün değildir. Buna göre, modafinil, döküntü açıkça ilaç ile ilgili değilse, döküntü ilk belirtisinde normal olarak kesilmelidir. Tedavinin kesilmesi, döküntülerin hayatı tehdit etmesini veya kalıcı olarak devre dışı bırakılmasını veya şekil değiştirmesini önlemeyebilir.
Anjiyoödem ve Anafilaktoid Reaksiyonlar
Bir ciddi anjiyoödem vakası ve bir aşırı duyarlılık vakası (döküntü, disfaji ve bronkospazm ile) modafinil'in R enantiomeri olan armodafinil (rasemik olan) karışımı). Modafinil klinik çalışmalarında böyle bir vaka gözlenmemiştir. Bununla birlikte, modafinil ile pazarlama sonrası deneyimde anjiyoödem bildirilmiştir. Hastalara tedaviyi bırakmaları ve derhal doktorlarına herhangi bir belirti bildirmeleri tavsiye edilmelidir. veya anjiyoödem veya anafilaksi düşündüren semptomlar (örn. yüz, göz, dudak, dil veya larinks; yutma veya nefes almada zorluk; ses kısıklığı).
Çok Organlı Aşırı Duyarlılık Reaksiyonları
Pazarlama sonrası deneyimde en az bir ölüm içeren çok organlı aşırı duyarlılık reaksiyonları, başlangıcına kadar yakın temporal ilişkilendirmede (medyanın saptanması için ortalama süre 13 gün: aralık 4-33) meydana geldi modafinil.
Sınırlı sayıda rapor olmasına rağmen, çok organlı aşırı duyarlılık reaksiyonları hastaneye yatma veya yaşamı tehdit edici olabilir. Modafinil ile ilişkili çok organlı aşırı duyarlılık reaksiyonlarının ciddiyetini veya şiddetini öngördüğü bilinen hiçbir faktör yoktur. Bu bozukluğun belirti ve semptomları çeşitlidir; bununla birlikte, hastalar tipik olarak, sadece olmasa da, diğer organ sistemi tutulumu ile ilişkili ateş ve döküntü ile başvurmuşlardır. İlişkili diğer belirtiler arasında miyokardit, hepatit, karaciğer fonksiyon testi anormallikleri, hematolojik anormallikler (örn. eozinofili, lökopeni, trombositopeni), kaşıntı ve astenidir. Çok organlı aşırı duyarlılık ifadesinde değişken olduğundan, burada belirtilmeyen diğer organ sistemi semptom ve bulguları ortaya çıkabilir.
Çok organlı aşırı duyarlılık reaksiyonundan şüpheleniliyorsa Provigil kesilmelidir. Bu sendromu üreten diğer ilaçlarla çapraz duyarlılığı gösteren vaka raporları olmamasına rağmen, çoklu organ aşırı duyarlılığı ile ilişkili ilaçlarla ilgili deneyim, bunun bir olasılık.
Kalıcı Uyku hali
Provigil alan anormal uyku hali olan hastalara uyanıklık düzeylerinin normale dönmeyebileceği bildirilmelidir. Provigil alan hastalar da dahil olmak üzere aşırı uyku hali olan hastalar, uykusuzluk derecesi ve uygunsa, sürüşten veya potansiyel olarak tehlikeli herhangi bir faaliyetten kaçınması önerilir. Reçete yazan kişiler ayrıca, belirli faaliyetler sırasında uyuşukluk veya uykusuzluk hakkında doğrudan sorgulanana kadar hastaların uyuklama veya uyuşukluğu kabul edemeyeceğinin farkında olmalıdır.
Psikiyatrik Belirtiler
Modafinil ile tedavi edilen hastalarda psikiyatrik olumsuz deneyimler bildirilmiştir. Modafinil kullanımı ile ilişkili pazarlama sonrası advers olaylar mani, sanrılar, halüsinasyonlar, intihar düşüncesi ve saldırganlığı içerir, bazıları hastaneye yatmaya neden olur. Hepsi olmasa da birçoğunun daha önce psikiyatrik öyküsü vardı. Sağlıklı bir erkek gönüllü, günlük 600 mg'lık birden fazla modafinil ve uyku yoksunluğu ile birlikte referans, paranoid sanrılar ve işitsel halüsinasyonlar geliştirdi. İlaç kesildikten 36 saat sonra psikoz kanıtı yoktu.
Erişkin modafinil kontrollü çalışma veritabanında, tedavinin kesilmesine neden olan psikiyatrik semptomlar (>% 0,3 sıklıkta) ve hastalarda daha sık bildirilmiştir plasebo ile tedavi edilenlere kıyasla modafinil ile tedavi edilenler anksiyete (% 1), sinirlilik (% 1), uykusuzluk (
üst
Önlemler
Uyku Bozukluklarının Teşhisi
Provigil sadece aşırı uykululuklarının tam bir değerlendirmesini yapmış olan ve Narkolepsi, OSAHS ve / veya SWSD tanısı ICSD veya DSM tanı kriterlerine göre konulmuştur (Bkz. Klinik İzler). Böyle bir değerlendirme genellikle tam bir öykü ve fizik muayeneden oluşur ve bir laboratuvar ortamında testlerle desteklenebilir. Bazı hastalarda aşırı uykululuklarına katkıda bulunan birden fazla uyku bozukluğu olabilir (örneğin, aynı hastada çakışan OSAHS ve SWSD).
Genel
Modafinil'in fonksiyonel bozukluk ürettiği gösterilmemesine rağmen, CNS'yi etkileyen herhangi bir ilaç yargı, düşünme veya motor becerilerini değiştirebilir. Hastalar, bir otomobilin veya diğer tehlikeli makinelerin çalıştırılmasında dikkatli olunmalıdır. Provigil tedavisinin böyle bir tedaviye girme yeteneklerini olumsuz etkilemeyeceğinden emin olun faaliyetleri.
OSAHS Hastalarında CPAP Kullanımı
OSAHS'da Provigil, altta yatan tıkanıklık için standart tedaviye / tedavilere ek olarak endikedir. Sürekli pozitif hava yolu basıncı (CPAP) bir hasta için tercih edilen tedavi yöntemiyse, Provigil'i başlatmadan önce CPAP ile yeterli bir süre tedavi etmek için azami çaba gösterilmelidir. Provigil, CPAP ile yardımcı olarak kullanılıyorsa, CPAP uyumunun teşvik edilmesi ve periyodik olarak değerlendirilmesi gerekir.
Kardiyovasküler sistem
Modafinil, yakın geçmişte miyokard enfarktüsü veya kararsız angina öyküsü olan hastalarda değerlendirilmemiştir ve bu tür hastalar dikkatle tedavi edilmelidir.
Provigil klinik çalışmalarında, göğüs ağrısı, çarpıntı, nefes darlığı ve geçici iskemik dahil belirti ve bulgular Mitral kapak prolapsusu veya sol ventrikül ile ilişkili üç olguda EKG'de T dalgası değişiklikleri gözlendi hipertrofisi. Provigil tabletlerin sol ventrikül hipertrofisi öyküsü olan hastalarda veya Daha önce CNS alırken mitral kapak prolapsusu sendromu yaşayan mitral kapak prolapsusu olan hastalar uyarıcılar. Bu tür belirtiler, bunlarla sınırlı olmamak üzere, iskemik EKG değişiklikleri, göğüs ağrısı veya aritmi içerebilir. Bu semptomlardan herhangi birinin yeni başlangıcı meydana gelirse, kardiyak değerlendirmeyi düşünün.
Kısa süreli (<3 ay) kontrollü çalışmalarda kan basıncı izleme klinik olarak anlamlı değildi Provigil alan hastalarda ortalama sistolik ve diyastolik kan basıncındaki değişiklikler Plasebo. Bununla birlikte, bu çalışmalarda antihipertansif ilaç kullanımının retrospektif bir analizi, Provigil hastaları, plasebo hastalarına (% 0.7) kıyasla yeni veya artmış antihipertansif ilaçların (% 2.4) kullanımını gerektirdi. Sadece OSAHS çalışmaları dahil edildiğinde diferansiyel kullanım biraz daha büyüktü ve hastaların% 3.4'ü Provigil ve antihipertansif kullanımında bu tür değişiklikler gerektiren plasebo kullanan hastaların% 1.1'i ilaç. Provigil hastalarında kan basıncının daha fazla izlenmesi uygun olabilir.
Steroid Kontraseptif Kullanan Hastalar
Steroidal kontraseptiflerin etkinliği Provigil tabletleri ile kullanıldığında ve tedavinin kesilmesinden sonra bir ay boyunca azaltılabilir (Bkz. Önlemler, İlaç etkileşimleri). Provigil tabletleri ile tedavi edilen hastalar için ve Provigil'in kesilmesinden sonra bir ay boyunca alternatif veya eşzamanlı doğum kontrol yöntemleri önerilir.
Siklosporin kullanan hastalar
Provigil ile kullanıldığında kan siklosporin seviyeleri düşebilir (Bkz. Önlemler, İlaç etkileşimleri). Bu ilaçlar eş zamanlı kullanıldığında, dolaşımdaki siklosporin konsantrasyonlarının izlenmesi ve siklosporin için uygun doz ayarlaması düşünülmelidir.
Şiddetli Karaciğer Yetmezliği Olan Hastalar
Şiddetli karaciğer yetmezliği olan, sirozu olan veya olmayan hastalarda (Bkz. Klinik Farmakoloji), Provigil düşük dozda uygulanmalıdır (Bkz. Dozaj ve Uygulama).
Şiddetli Böbrek yetmezliği olan hastalar
Şiddetli böbrek yetmezliği olan hastalarda dozun güvenliğini ve etkinliğini belirlemek için yeterli bilgi yoktur. (Böbrek yetmezliğinde farmakokinetik için bkz. Klinik Farmakoloji.)
Yaşlı hastalar
Yaşlı hastalarda, modafinil ve metabolitlerinin ortadan kaldırılması yaşlanmanın bir sonucu olarak azaltılabilir. Bu nedenle, bu popülasyonda daha düşük dozların kullanımına dikkat edilmelidir. (Görmek Klinik Farmakoloji ve Dozaj ve Uygulama).
Hastalar İçin Bilgiler
Doktorlara, Provigil'i reçete ettikleri hastalarla aşağıdaki konuları tartışmaları tavsiye edilir.
Provigil, anormal düzeyde uyku hali olan hastalar için endikedir. Provigil'in iyileştiği gösterilmiştir, ancak bu anormal uykuya dalma eğilimini ortadan kaldırmamıştır. Bu nedenle, hastalar potansiyel olarak tehlikeli faaliyetler (örneğin, sürüş, makine kullanımı) veya diğer konularla ilgili önceki davranışlarını değiştirmemelidir. Provigil ile tedavinin buna izin veren uyanıklık seviyeleri ürettiği gösterilinceye kadar uygun uyanıklık seviyeleri gerektiren faaliyetler faaliyetleri. Hastalara Provigil'in uyku yerine geçmediği bildirilmelidir.
Hastalar, daha önce reçete edilen tedavilerini almaya devam etmelerinin kritik olabileceği konusunda bilgilendirilmelidir (ör. CPAP alan OSAHS hastaları bunu yapmaya devam etmelidir).
Hastalar hasta bilgi broşürünün mevcudiyeti hakkında bilgilendirilmeli ve Provigil'i almadan önce broşürü okumaları konusunda bilgilendirilmelidir.
Hastalara göğüs ağrısı, döküntü, depresyon, anksiyete veya psikoz veya mani belirtileri yaşarsa doktorlarıyla iletişime geçmeleri tavsiye edilmelidir.
Gebelik
Hastalara, hamile kalmaları veya tedavi sırasında gebe kalmayı planlamaları durumunda doktorlarını bilgilendirmeleri tavsiye edilmelidir. Steroid kontraseptifler (depo veya implante edilebilirler) kullanırken hastalar potansiyel hamilelik riski konusunda uyarılmalıdır. kontraseptifler) ile Provigil ile ve tedavinin kesilmesinden sonra bir ay boyunca (Bkz. Kanserojenez, Mutajenez, Doğurganlık Bozukluğu ve Gebelik).
hemşirelik
Hastalara, bir bebeği emziriyorlarsa doktorlarını bilgilendirmeleri tavsiye edilmelidir.
Eşzamanlı İlaç
Herhangi bir hasta alıp almayı veya almayı planlıyorlarsa, hastalara doktorlarını bilgilendirmeleri tavsiye edilmelidir. reçeteli veya reçetesiz satılan ilaçlar, çünkü Provigil ve diğer uyuşturucular.
Alkol
Hastalara Provigil'in alkolle kombinasyon halinde kullanımının incelenmediği bildirilmelidir. Hastalara Provigil kullanırken alkolden kaçınmanın ihtiyatlı olduğu bildirilmelidir.
Alerjik reaksiyonlar
Hastalara Provigil almayı bırakmaları ve döküntü gelişirse doktorlarını bilgilendirmeleri tavsiye edilmelidir. kurdeşen, ağız yaraları, kabarcıklar, cilt soyma, yutma veya nefes almada zorluk veya ilgili alerjik olgu.
İlaç etkileşimleri
CNS Aktif İlaçları
Metilfenidat
Sağlıklı gönüllülerde yapılan tek dozlu bir çalışmada, modafinil (200 mg) ile eşzamanlı uygulama metilfenidat (40 mg), herhangi birinin farmakokinetiğinde önemli bir değişikliğe neden olmamıştır. ilaç. Bununla birlikte, Provigil'in emilimi, metilfenidat ile birlikte uygulandığında yaklaşık bir saat geciktirilebilir.
Sağlıklı gönüllülerde yapılan çok dozlu, kararlı durum çalışmasında, modafinil 7 gün boyunca günde bir kez 200 mg / gün, ardından 21 gün boyunca 400 mg / gün uygulandı. Modafinil tedavisinin 22-28 günlerinde 8 saat sonra metilfenidat (20 mg / gün) uygulanması günlük modafinil dozu farmakokinetikte önemli bir değişikliğe neden olmamıştır. modafinil.
dekstroamfetamin
Sağlıklı gönüllülerde yapılan tek dozlu bir çalışmada, modafinil (200 mg) ile eşzamanlı uygulama dekstroamphetamin (10 mg), herhangi birinin farmakokinetiğinde önemli bir değişikliğe neden olmadı ilaç. Bununla birlikte, Provigil emilimi, dekstroamphetamin ile birlikte uygulandığında yaklaşık bir saat geciktirilebilir.
Sağlıklı gönüllülerde yapılan çok dozlu, kararlı durum çalışmasında, modafinil 7 gün boyunca günde bir kez 200 mg / gün, ardından 21 gün boyunca 400 mg / gün uygulandı. Modafinil tedavisinin 22-28. Günlerinde 7 saat sonra dekstroamphetamin (20 mg / gün) uygulanması günlük modafinil dozu farmakokinetikte önemli bir değişikliğe neden olmamıştır. modafinil.
Clomipramine
Üç günlük tedavinin ilk gününde tek bir doz klomipraminin (50 mg) birlikte uygulanması sağlıklı gönüllülerde modafinil (200 mg / gün) her iki ilacın farmakokinetiği üzerinde bir etki göstermemiştir. Bununla birlikte, modafinil tedavisi sırasında narkolepsili bir hastada artmış klomipramin ve aktif metaboliti desmetilklomipramin düzeylerinde bir olay bildirilmiştir.
Trizolam
Provigil ve etinil estradiol (EE2) arasındaki ilaç etkileşimi çalışmasında, EE2 farmakokinetiği için plazma örneklemesi, tek bir doz triazolam (0.125 mg) da uygulandı. Triazolamın ortalama Cmax ve AUC0-respectively değerleri sırasıyla% 42 ve% 59 azaldı ve eliminasyon yarılanma ömrü, modafinil tedavisinden yaklaşık bir saat sonra azaldı.
Monoamin Oksidaz (MAO) İnhibitörleri
Monoamin oksidaz inhibitörleri ile etkileşim çalışmaları yapılmamıştır. Bu nedenle, MAO inhibitörleri ve modafinil ile birlikte uygulanırken dikkatli olunmalıdır.
Diğer uyuşturucular
Warfarin
Tek bir rasemik varfarin (5 mg) verildiğinde sağlıklı deneklerde R ve S-varfarinin farmakokinetik profillerinde önemli bir değişiklik olmamıştır. modafinil'in (7 gün boyunca 200 mg / gün, ardından 27 gün boyunca 400 mg / gün) kronik verilmesini takiben verilen deneklere göre profiller Plasebo. Bununla birlikte, Provigil varfarin ile birlikte uygulandığında protrombin sürelerinin / INR'nin daha sık izlenmesi önerilir (Bkz. Klinik Farmakoloji, Farmakokinetik, İlaç-İlaç Etkileşimleri).
Etinil Estradiol
Modafinil'in 7 gün boyunca günde bir kez 200 mg / gün kadın gönüllülere uygulanması ve ardından 400 21 gün boyunca mg / gün, etinil estradiolün Cmax değerinde ortalama% 11 azalma ve AUC0-24'te% 18 azalma ile sonuçlandı (EE2; 0.035 mg; norgestimate ile oral yoldan uygulanır). Etinil estradiolün eliminasyon oranında belirgin bir değişiklik olmamıştır.
Siklosporin
Organ nakli yapılan 41 yaşındaki bir kadında modafinil ile CYP3A4'ün bir substratı olan siklosporin arasında bir etkileşim vakası bildirilmiştir. Bir aylık 200 mg / gün modafinil uygulamasından sonra siklosporin kan seviyeleri% 50 azalmıştır. Etkileşimin, siklosporinin artan metabolizmasından kaynaklandığı varsayılmıştır, çünkü ilacın düzenini etkilemesi beklenen başka bir faktör değişmemiştir. Siklosporin için dozaj ayarlaması gerekebilir.
Sitokrom P-450 İzoenzimler ve Diğer Hepatik Enzimlerle İnhibe Eden, İndükleyen veya Metabolize Olan İlaçlarla Potansiyel Etkileşimler
Primer insan hepatosit kültürlerini kullanan in vitro çalışmalarda, modafinilin konsantrasyona bağlı bir şekilde hafifçe CYP1A2, CYP2B6 ve CYP3A4'ü indüklediği gösterilmiştir. Her ne kadar in vitro deneylere dayanan indüksiyon sonuçları in vivo yanıtı öngörmek zorunda olmasa da, dikkat Provigil, bu üç enzime bağımlı olan ilaçlarla birlikte uygulandığında Boşluk. Özellikle, bu tür ilaçların daha düşük kan seviyeleri ortaya çıkabilir (Bkz. Diğer İlaçlar, Siklosporineabove).
İnsan hepatositlerinin in vitro modafinil'e maruz kalması CYP2C9 aktivitesinin ekspresyonunun belirgin bir konsantrasyonla ilişkili baskılanmasına neden oldu modafinil ile bu enzimin substratları arasında metabolik bir etkileşim potansiyeli olduğunu düşündürmektedir (örneğin, S-varfarin ve fenitoin). Sağlıklı gönüllülerde yapılan daha sonraki bir klinik çalışmada, kronik modafinil tedavisi, varfarinin tek doz farmakokinetiği üzerinde plaseboya kıyasla anlamlı bir etki göstermemiştir (bkz. Önlemler, İlaç Etkileşimleri, Warfarin).
İnsan karaciğer mikrozomlarını kullanan in vitro çalışmalar, modafinilin CYP2C19'u farmakolojik olarak ilgili modafinil konsantrasyonlarında geri dönüşümlü olarak inhibe ettiğini gösterdi. CYP2C19 da benzer bir kuvvetle dolaşımdaki bir metabolit olan modafinil sülfon tarafından geri dönüşümlü olarak inhibe edilir. Modafinil sülfonun maksimum plazma konsantrasyonları ebeveyninkinden çok daha düşük olmasına rağmen modafinil, her iki bileşiğin birleşik etkisi, sürekli kısmi inhibisyon üretebilir. enzim. Diazepam, propranolol, fenitoin (ayrıca CYP2C9 yoluyla) gibi CYP2C19 metabolizması ile büyük ölçüde elimine edilen ilaçlar veya S-mepenitoin, Provigil ile birlikte uygulama üzerine uzun süreli eliminasyon yapmış olabilir ve dozajın azaltılmasını ve izlenmesini gerektirebilir toksisite için.
Trisiklik antidepresanlar
CYP2C19 ayrıca öncelikle CYP2D6 tarafından metabolize edilen bazı trisiklik antidepresanların (örn., Klomipramin ve desipramin) metabolizması için yardımcı bir yol sağlar. CYP2D6 eksikliği olan trisiklik ile tedavi edilen hastalarda (yani, debrisokinin zayıf metabolizörleri olanlar; Kafkas nüfusunun% 7-10'u; benzer veya diğer popülasyonlarda daha düşük), CYP2C19 tarafından metabolizma miktarı önemli ölçüde arttırılabilir. Provigil, bu hasta alt grubunda trisiklik seviyelerinin yükselmesine neden olabilir. Doktorlar, bu hastalarda trisiklik ajanların dozunda bir azalmanın gerekli olabileceğinin farkında olmalıdır.
Ek olarak, CYP3A4'ün modafinil'in metabolik eliminasyonuna kısmi katılımı nedeniyle, güçlü CYP3A4 indükleyicilerinin birlikte uygulanması (örn. karbamazepin, fenobarbital, rifampin) veya CYP3A4 inhibitörleri (örn. ketokonazol, itrakonazol) plazma seviyelerini değiştirebilir. modafinil.
Karsinogenez, Mutajenez, Doğurganlık Bozukluğu
Karsinogenezin
Diyette modafinil'in 78 hafta boyunca farelere ve sıçanlara 6, 30 ve 60 mg / kg / gün dozlarında 104 hafta boyunca uygulandığı karsinojenisite çalışmaları yapılmıştır. Çalışılan en yüksek doz, mg / m2 bazında önerilen yetişkin insan günlük modafinil dozundan (200 mg) 1.5 (fare) veya 3 (sıçan) kat daha fazladır. Bu çalışmalarda modafinil uygulamasıyla ilişkili tümör oluşumu kanıtı yoktu. Bununla birlikte, fare çalışması, maksimum tolere edilen bir dozu temsil etmeyen, yetersiz bir yüksek doz kullandığı için, daha sonra Tg'de kanserojenlik çalışması yapılmıştır. AC transgenik fare. Tg. AC analizi, dermal olarak uygulanan 125, 250 ve 500 mg / kg / gün idi. Modafinil uygulamasıyla ilişkili tümör oluşumuna dair bir kanıt yoktu; bununla birlikte, bu dermal model oral yoldan verilen bir ilacın kanserojen potansiyelini yeterince değerlendirmeyebilir.
Mutajenez
Modafinil, bir dizi in vitro (yani bakteriyel ters mutasyon deneyi, fare lenfoma tk deneyi, kromozomal aberasyon) içerisinde mutajenik veya klastojenik potansiyel kanıtı göstermedi insan lenfositlerinde analiz, BALB / 3T3 fare embriyo hücrelerinde hücre dönüşüm analizi) metabolik aktivasyonun yokluğunda veya varlığında analizler veya in vivo (fare kemik iliği mikronükleusu) tahliller. Modafinil ayrıca sıçan hepatositlerinde planlanmamış DNA sentezi analizinde negatifti.
Doğurganlığın Bozulması
Erkek ve dişi sıçanlara modafinil (480 mg / kg / güne kadar dozlar) öncesinde ve boyunca oral uygulama çiftleşme ve gestasyonun 7. gününe kadar kadınlarda devam etmek, en yüksek çiftleşme zamanında bir artışa neden oldu. doz; diğer doğurganlık veya üreme parametreleri üzerinde herhangi bir etki gözlenmemiştir. 240 mg / kg / gün etkisiz doz, önerilen 200 mg'lık dozda insanlardakine yaklaşık olarak eşit bir plazma modafinil maruziyeti (EAA) ile ilişkilendirilmiştir.
Gebelik
Gebelik Kategorisi C:
Sıçan ve tavşanlarda yapılan çalışmalarda klinik olarak anlamlı maruziyetlerde gelişimsel toksisite gözlenmiştir.
Modafinil (50, 100 veya 200 mg / kg / gün), gebe sıçanlara organogenez döneminde ağızdan uygulanan maternal toksisite, rezorpsiyonlarda artış ve en yüksek yavrularda visseral ve iskelet varyasyonları insidansında artış doz. Sıçan embriyofetal gelişim toksisitesi için daha yüksek etkisiz doz, bir plazma ile ilişkiliydi modafinil maruziyeti önerilen günlük dozda (RHD) insanlarda AUC'nin yaklaşık 0.5 katı 200 mg. Bununla birlikte, 480 mg / kg / gün'e kadar olan bir sonraki çalışmada (RHD'de insanlarda AUC'nin yaklaşık 2 katı plazma modafinil maruziyeti) embriyofetal gelişim üzerinde hiçbir olumsuz etki gözlenmemiştir.
Modafinil, organogenez döneminde 45, 90 dozlarında hamile tavşanlara oral olarak uygulanır ve 180 mg / kg / gün, fetal yapısal değişiklikler ve embriyofetal ölüm vakalarını en yüksek dozda artırmıştır. Gelişimsel toksisite için en yüksek etkisiz doz, RHD'de insanlarda yaklaşık AUC'ye eşit bir plazma modafinil AUC ile ilişkiliydi.
Armodafinil (modafinil'in R-enantiyomeri) oral uygulaması; 60, 200 veya 600 mg / kg / gün) organogenez süresi boyunca gebe sıçanlara, orta dozda veya daha yüksek fetal viseral ve iskelet varyasyonları ve en yüksek fetal vücut ağırlıklarında azalma doz. Sıçan embriyofetal gelişim toksisitesi için etkisiz doz, bir plazma armodafinil ile ilişkiliydi maruz kalma (AUC), modafinil ile tedavi edilen insanlarda armodafinil için AUC'nin onda biri kadar RHD.
Modafinil, 200 mg / kg / gün'e kadar oral dozlarda gebelik ve emzirme döneminde sıçanlara uygulama ile azaldı 20 mg / kg / gün'den daha yüksek dozlarda yavrularda canlılık (plazma modafinil EAA, insanlarda EAA'nın yaklaşık 0.1 katıdır. RHD). Hayatta kalan yavrularda doğum sonrası gelişimsel ve nörodavranışsal parametreler üzerinde herhangi bir etki gözlenmemiştir.
Gebe kadınlarda yeterli ve iyi kontrollü çalışma yoktur. Armodafinil ve modafinil ile ilişkili olarak iki intrauterin gelişme geriliği ve bir spontan düşük vakası bildirilmiştir. Modafinil ve armodafinil farmakolojisi sempatomimetik aminlerinki ile aynı olmasa da, bu sınıfla bazı farmakolojik özellikleri paylaşırlar. Bu ilaçların bazıları intrauterin gelişme geriliği ve spontan düşüklerle ilişkilendirilmiştir. Bildirilen vakaların uyuşturucuya bağlı olup olmadığı bilinmemektedir.
Modafinil hamilelik sırasında sadece potansiyel fayda fetusun potansiyel riskini haklı çıkarsa kullanılmalıdır.
Emek ve Teslimat
Modafinilin insanlarda doğum ve doğum üzerindeki etkisi sistematik olarak araştırılmamıştır.
Emziren Anneler
Modafinil veya metabolitlerinin anne sütüne geçip geçmediği bilinmemektedir. Birçok ilaç anne sütüne geçtiği için, Provigil tabletleri emziren bir kadına uygulandığında dikkatli olunmalıdır.
Pediyatrik Kullanım
16 yaş altı pediatrik hastalarda güvenlik ve etkinlik belirlenmemiştir. Eritema multiforme major (EMM) ve Stevens-Johnson Sendromu (SJS) dahil olmak üzere ciddi deri döküntüleri pediatrik hastalarda modafinil kullanımı ile ilişkilendirilmiştir (bkz. Uyarılar, Stevens-Johnson Sendromu dahil Ciddi Döküntü).
Kontrollü 6 haftalık bir çalışmada narkolepsili 165 pediatrik hasta (5-17 yaş) modafinil (n = 123) veya plasebo (n = 42) ile tedavi edildi. Uyku gecikmesini uzatmak için modafinil'i plaseboya tercih eden istatistiksel olarak anlamlı bir fark yoktu. MSLT ile ölçülen veya klinik global izlenim-klinisyen ölçeği ile belirlenen uyku hali algılarında ölçülen (CGI-C).
Kontrollü ve açık etiketli klinik çalışmalarda, psikiyatrik ve sinir sisteminin ortaya çıkan yan etkileri Tourette sendromu, uykusuzluk, düşmanlık, artmış katapleksi, artan hipnagojik halüsinasyonlar ve intihar dahil düşüncesi. Tıbbi müdahale olmadan düzelen geçici lökopeni de gözlenmiştir. Kontrollü klinik çalışmada, modafinil ile tedavi edilen 12 yaş ve üstü 38 kızdan 3'ünde plasebo alan 10 kızdan 0'ında dismenore görülmüştür.
Geriyatrik Kullanım
65 yaş üstü bireylerde güvenlik ve etkinlik belirlenmemiştir. Klinik çalışmalarda 65 yaşın üzerindeki sınırlı sayıda hastada deneyim, diğer yaş gruplarına benzer olumsuz deneyimler görülmüştür.
üst
Ters tepkiler
Modafinil, 2000'den fazla aşırı hastası olan 3500'den fazla hastada güvenlik açısından değerlendirilmiştir. birincil uyku ve uyanıklık bozuklukları ile ilişkili uyku hali en az bir doz modafinil. Klinik çalışmalarda modafinil'in genel olarak iyi tolere edildiği ve olumsuz deneyimlerin çoğunun hafif ila orta derecede olduğu bulunmuştur.
Plasebo kontrollü plasebo ile tedavi edilen hastalardan daha sık Provigil kullanımı ile ilişkili en sık görülen advers olaylar (â ‰ ¥ 5%) uyku ve uyanıklığın birincil bozukluklarında klinik çalışmalar baş ağrısı, bulantı, sinirlilik, rinit, ishal, sırt ağrısı, anksiyete, uykusuzluk, baş dönmesi ve hazımsızlık. Bu çalışmalarda advers olay profili benzerdi.
Plasebo kontrollü klinik çalışmalarda, Provigil alan 934 hastanın 74'ü (% 8), plasebo alan hastaların% 3'üne kıyasla olumsuz bir deneyim nedeniyle kesildi. Provigil için plasebodan daha yüksek bir oranda ortaya çıkan en sık bırakma nedenleri hastalar baş ağrısı (% 2), bulantı, anksiyete, baş dönmesi, uykusuzluk, göğüs ağrısı ve sinirlilikti (her biri <1%). Kanadalı bir klinik çalışmada, daha önce senkopal atak öyküsü olan 35 yaşında obez narkoleptik bir erkek 27 günlük modafinil tedavisinden sonra 9 saniyelik bir asistol atağı yaşadı (bölünmüş olarak 300 mg / gün doz).
Kontrollü Araştırmalarda Görülme Sıklığı
Aşağıdaki tablo (Tablo 3),% 1 veya daha fazla bir oranda meydana gelen ve daha sık görülen olumsuz deneyimleri göstermektedir. Provigil ile tedavi edilen yetişkin hastalarda, ana, plasebo kontrollü klinikte plasebo ile tedavi edilen hastalara göre denemeler.
Reçete yazan kişi, aşağıda verilen rakamların, hastalardaki olumsuz deneyimlerin sıklığını tahmin etmek için kullanılamayacağının farkında olmalıdır. Hasta özelliklerinin ve diğer faktörlerin klinik sırasında ortaya çıkanlardan farklı olabileceği olağan tıbbi uygulamanın seyri çalışmaları. Benzer şekilde, belirtilen frekanslar, farklı tedaviler, kullanımlar veya araştırmacıları içeren diğer klinik araştırmalardan elde edilen rakamlarla doğrudan karşılaştırılamaz. Bununla birlikte, bu sıklıkların gözden geçirilmesi, reçete yazanlara, incelenen popülasyondaki advers olayların insidansına ilaç ve ilaç dışı faktörlerin göreceli katkısını tahmin etme temeli sağlar.
| Vücut sistemi | Tercih Edilen Terim | modafinil (n = 934) |
plasebo (n = 567) |
| * Narkolepsi, OSAHS ve SWSD'de altı çift kör, plasebo kontrollü klinik çalışma. 1 Provigil ile tedavi edilen hastaların en az% 1'inin plasebo grubundan daha sık bildirdiği olaylar; insidans en yakın% 1'e yuvarlanır. Olumsuz deneyim terminolojisi standart değiştirilmiş COSTART Sözlüğü kullanılarak kodlanır. Provigil insidansı en az% 1, ancak plaseboya eşit veya daha az olan olaylar tabloda listelenmemiştir. Bu olaylar şunları içerir: enfeksiyon, ağrı, kazayla yaralanma, karın ağrısı, hipotermi, alerjik reaksiyon, asteni, ateş, viral enfeksiyon, boyun ağrısı, migren, anormal elektrokardiyogram, hipotansiyon, diş bozukluğu, kusma, periodontal apse, artan iştah, ekimoz, hiperglisemi, periferik ödem, kilo kaybı, ağırlık kazanç, kas ağrısı, bacak krampları, artrit, katapleksi, düşünme anormalliği, uyku bozukluğu, öksürük, sinüzit, dispne, bronşit, döküntü, konjonktivit, kulak ağrısı, dismenore4, idrar yolu enfeksiyonu. 2 Yüksek karaciğer enzimleri. 3 Oro-yüz diskinezileri. 4 İnsidans cinsiyete göre ayarlandı. | |||
| Bir bütün olarak beden | Baş ağrısı | 34% | 23% |
| Sırt ağrısı | 6% | 5% | |
| Grip Sendromu | 4% | 3% | |
| Göğüs ağrısı | 3% | 1% | |
| Titreme | 1% | 0% | |
| Boyun Sertliği | 1% | 0% | |
| Kardiyovasküler | Hipertansiyon | 3% | 1% |
| taşikardi | 2% | 1% | |
| Çarpıntı | 2% | 1% | |
| vazodilatasyon | 2% | 0% | |
| Sindirim | Mide bulantısı | 11% | 3% |
| İshal | 6% | 5% | |
| hazımsızlık | 5% | 4% | |
| Kuru ağız | 4% | 2% | |
| anoreksi | 4% | 1% | |
| Kabızlık | 2% | 1% | |
| Anormal Karaciğer Fonksiyonu2 | 2% | 1% | |
| tantana | 1% | 0% | |
| Ağız Ülserasyonu | 1% | 0% | |
| Susuzluk | 1% | 0% | |
| Hemic / Lenf | Eozinofili | 1% | 0% |
| Metabolik / Beslenme | Ödem | 1% | 0% |
| Sinirli | Sinirlilik | 7% | 3% |
| Uykusuzluk hastalığı | 5% | 1% | |
| kaygı | 5% | 1% | |
| Baş dönmesi | 5% | 4% | |
| Depresyon | 2% | 1% | |
| Parestezi | 2% | 0% | |
| uyuklama | 2% | 1% | |
| hipertoni | 1% | 0% | |
| Diskinezisi3 | 1% | 0% | |
| hiperkinezi | 1% | 0% | |
| Çalkalama | 1% | 0% | |
| karışıklık | 1% | 0% | |
| titreme | 1% | 0% | |
| Duygusal Labilite | 1% | 0% | |
| baş dönmesi | 1% | 0% | |
| Solunum | Rinit | 7% | 6% |
| Farenjit | 4% | 2% | |
| Akciğer Bozukluğu | 2% | 1% | |
| Epistaksis | 1% | 0% | |
| Astım | 1% | 0% | |
| Cilt / ekleri | Terlemek | 1% | 0% |
| Herpes Simpleks | 1% | 0% | |
| Özel Duyular | Ambliyopi | 1% | 0% |
| Anormal Görme | 1% | 0% | |
| Lezzet Sapkınlığı | 1% | 0% | |
| Göz ağrısı | 1% | 0% | |
| Ürogenital | İdrar Bozukluğu | 1% | 0% |
| hematüri | 1% | 0% | |
| Piyüri | 1% | 0% |
Olumsuz Olayların Doz Bağımlılığı
200, 300 ve 400 mg / gün dozlarını karşılaştıran yetişkin plasebo kontrollü klinik çalışmalarda Provigil ve plasebo, açıkça dozla ilişkili olan tek olumsuz olay baş ağrısı ve kaygı.
Hayati İşaret Değişiklikleri
Ortalama kalp hızı veya sistolik ve diyastolik kan basıncı değerlerinde tutarlı bir değişiklik olmamasına rağmen, Provigil kullanan hastalarda antihipertansif ilaç gereksinimi plaseboya kıyasla biraz daha fazlaydı (Bkz. Önlemler).
Kilo Değişimi
Provigil ile tedavi edilen hastalarda, plasebo kontrollü klinik çalışmalarda plasebo ile tedavi edilen hastalara kıyasla, vücut ağırlığı değişikliğinde klinik olarak anlamlı bir fark yoktu.
Laboratuvar Değişiklikleri
Faz 1, 2 ve 3 çalışmalarda klinik kimya, hematoloji ve idrar tahlili parametreleri izlendi. Bu çalışmalarda, plazmadan değil Provigil uygulamasından sonra ortalama gama glutamiltransferaz (GGT) ve alkalin fosfataz (AP) plazma düzeylerinin daha yüksek olduğu bulundu. Bununla birlikte, bazı deneklerde normal aralığın dışında GGT veya AP yükselmeleri vardı. Faz 3 klinik çalışmalarında Provigil ile tedavi edilen popülasyonda zamanla daha yüksek, ancak klinik olarak anlamlı olmayan anormal değil, GGT ve AP değerlerinin arttığı görülmüştür. Alanin aminotransferaz, aspartat aminotransferaz, toplam protein, albümin veya toplam bilirubin arasında fark yoktu.
EKG Değişiklikleri
Provigil uygulamasını takiben plasebo kontrollü klinik çalışmalarda tedaviye bağlı EKG anormallikleri saptanmadı.
Pazarlama Sonrası Raporlar
Provigil'in onay sonrası kullanımı sırasında aşağıdaki advers reaksiyonlar tanımlanmıştır. Bu reaksiyonlar, belirsiz büyüklükteki bir popülasyondan gönüllü olarak bildirildiğinden, sıklıklarını güvenilir bir şekilde tahmin etmek veya ilaç maruziyeti ile nedensel bir ilişki kurmak mümkün değildir. Bu reaksiyonları etiketlemeye dahil etme kararları tipik olarak aşağıdaki faktörlerden bir veya daha fazlasına dayanır: (1) reaksiyonun ciddiyeti, (2) raporlamanın sıklığı veya (3) Provigil.
Hematolojik: agranülositoz
üst
Uyuşturucu Kullanımı ve Bağımlılığı
Kontrollü Madde Sınıfı
Modafinil (Provigil), Kontrollü Maddeler Kanununun Çizelge IV'ünde listelenmiştir.
Kötüye Kullanım Potansiyeli ve Bağımlılığı
İnsanlarda uyanıklığı arttırıcı etkisine ve hayvanlarda, insanlarda artan lokomotor aktivitesine ek olarak Provigil, psikoaktif ve öforik etkiler, ruh halindeki değişiklikler, algı, düşünme ve diğer CNS uyarıcılarının tipik duyguları. In vitro bağlanma çalışmalarında, modafinil dopamin geri alım bölgesine bağlanır ve hücre dışı dopaminde bir artışa neden olur, ancak dopamin salımında bir artışa neden olmaz. Modafinil, daha önce kendi kendini yöneten kokain için eğitilmiş maymunlarda kendi kendine uygulama ile kanıtlandığı gibi güçlendiriyor. Bazı çalışmalarda, modafinil de uyarıcı benzeri olarak kısmen ayırt edilmiştir. Doktorlar, özellikle ilaç ve / veya uyarıcı (örn., Metilfenidat, amfetamin veya kokain) öyküsü olan hastaları yakından takip etmelidir. Hastalar kötüye kullanım veya kötüye kullanım belirtileri açısından gözlemlenmelidir (örn. Dozların artırılması veya ilaç arama davranışı).
Modafinil (200, 400 ve 800 mg) kötüye kullanım potansiyeli, istismar ilaçları ile deneyimli kişilerde yatan bir çalışmada metilfenidata (45 ve 90 mg) göre değerlendirilmiştir. Bu klinik çalışmanın sonuçları, modafinil'in diğer programlanmış CNS uyarıcıları (metilfenidat) ile uyumlu psikoaktif ve öforik etkiler ve duygular ürettiğini göstermiştir.
Para çekme
Modafinil yoksunluğunun etkileri, bir ABD Faz 3 kontrollü klinik çalışmada 9 haftalık modafinil kullanımının ardından izlenmiştir. Narkoleptik hastalarda uyku hali geri dönmesine rağmen, 14 günlük gözlem sırasında spesifik bir yoksunluk belirtisi gözlenmemiştir.
üst
Doz Aşımı
İnsan deneyimi
Klinik çalışmalarda, 1000 ila 1600 mg / gün arasında değişen toplam 151 protokol tanımlı doz (önerilen günlük dozun 5 ila 8 katı) 200 mg), 7 ila 21 ardışık süre boyunca 1000 veya 1200 mg / gün doz alan 13 hasta dahil 32 hastaya uygulandı. günler. Ek olarak, birkaç kasıtlı akut doz aşımı meydana geldi; en büyük ikisi 4500 mg ve 4000 mg olup, yabancı depresyon çalışmalarına katılan iki denek tarafından alınmıştır. Bu çalışma deneklerinin hiçbirinde beklenmedik veya hayatı tehdit eden herhangi bir etki görülmemiştir. Bu dozlarda bildirilen olumsuz deneyimler, uyarma veya ajitasyon, uykusuzluk ve hemodinamik parametrelerde hafif veya orta dereceli yükselmelerdi. Klinik çalışmalarda gözlenen diğer yüksek doz etkileri arasında anksiyete, sinirlilik, agresiflik, karışıklık, sinirlilik, titreme, çarpıntı, uyku bozuklukları, bulantı, ishal ve azalmış protrombin saati.
Pazarlama sonrası deneyimlerden, tek başına modafinil (12 grama kadar dozlar) içeren ölümcül aşırı doz rapor edilmemiştir. Modafinil dahil olmak üzere birden fazla ilacı içeren aşırı dozlar ölümcül sonuçlarla sonuçlanmıştır. Modafinil doz aşımına en sık eşlik eden semptomlar, tek başına veya diğer ilaçlarla birlikte şunları içerir: uykusuzluk; huzursuzluk, yönelim bozukluğu, konfüzyon, uyarılma ve halüsinasyon gibi merkezi sinir sistemi semptomları; mide bulantısı ve ishal gibi sindirim değişiklikleri; ve taşikardi, bradikardi, hipertansiyon ve göğüs ağrısı gibi kardiyovasküler değişiklikler.
11 aylıktan küçük çocuklarda kazara yutma / aşırı doz vakaları bildirilmiştir. Mg / kg bazında bildirilen en yüksek kazara yutma 800-1000 mg (50-63 mg / kg) modafinil alan üç yaşında bir çocukta meydana geldi. Çocuk sabit kaldı. Çocuklarda aşırı doz ile ilişkili semptomlar yetişkinlerde gözlenenlere benzerdi.
Doz aşımı yönetimi
Modafinil doz aşımının toksik etkilerine karşı spesifik bir antidot tespit edilmemiştir. Bu tür aşırı dozlar, kardiyovasküler izleme dahil olmak üzere öncelikle destekleyici bakım ile yönetilmelidir. Kontrendikasyon yoksa, uyarılmış kusma veya gastrik lavaj düşünülmelidir. İlaç eliminasyonunun arttırılmasında diyaliz veya idrar asidifikasyonu veya alkalinizasyonun kullanılmasını önerecek herhangi bir veri yoktur. Doktor, aşırı doz tedavisi için bir zehir kontrol merkezine başvurmayı düşünmelidir.
üst
Dozaj ve Uygulama
Önerilen Provigil dozu günde bir kez 200 mg'dır.
Narkolepsi ve OSAHS hastaları için, Provigil sabahları tek bir doz olarak alınmalıdır.
SWSD hastaları için Provigil, iş vardiyasının başlamasından yaklaşık 1 saat önce alınmalıdır.
Tek bir doz olarak verilen 400 mg / gün'e kadar olan dozlar iyi tolere edilmiştir, ancak bu dozun 200 mg dozunun ötesinde ek fayda sağladığına dair tutarlı bir kanıt yoktur (Bkz. Klinik Farmakoloji ve Klinik İzler).
Genel Değerlendirmeler
Triazolam ve siklosporin gibi CYP3A4 için substrat olan eşlik eden ilaçlar için dozaj ayarlaması düşünülmelidir (Bkz. Önlemler, İlaç etkileşimleri).
Diazepam, propranolol, fenitoin (ayrıca CYP2C9 yoluyla) gibi CYP2C19 metabolizması ile büyük ölçüde elimine edilen ilaçlar veya S-mepenitoin, Provigil ile birlikte uygulama üzerine uzun süreli eliminasyon yapmış olabilir ve dozajın azaltılmasını ve izlenmesini gerektirebilir toksisite için.
Şiddetli karaciğer yetmezliği olan hastalarda, Provigil dozu normal karaciğer fonksiyonuna sahip hastalar için önerilen dozun yarısına düşürülmelidir (Bkz.Klinik Farmakoloji ve Önlemler).
Şiddetli böbrek yetmezliği olan hastalarda dozlamanın güvenliğini ve etkinliğini belirlemek için yeterli bilgi yoktur (Bkz. Klinik Farmakoloji ve Önlemler).
Yaşlı hastalarda Provigil ve metabolitlerinin ortadan kaldırılması yaşlanmanın bir sonucu olarak azaltılabilir. Bu nedenle, bu popülasyonda daha düşük dozların kullanımına dikkat edilmelidir (Bkz. Klinik Farmakoloji ve Önlemler).
üst
Nasıl tedarik edildi
Provigil® (modafinil) Tabletler
100 mg: Kapsül şeklindeki, beyaz, kaplanmamış her tablet bir tarafta "Provigil" ve diğer tarafta "100 MG" ile karıştırılır.
NDC 63459-101-01 - 100 şişe
200 mg: Her kapsül şeklindeki, beyaz, çentikli, kaplanmamış tablet bir tarafta "Provigil" ve diğer tarafta "200 MG" ile karıştırılır.
NDC 63459-201-01 - 100 şişe
20 ° - 25 ° C (68 ° - 77 ° F) sıcaklıkta saklayın.
İçin üretildi:
Cephalon, Inc.
Frazer, PA 19355
ABD Patentleri No. RE37.516 / 4.927.855
© Cephalon, Inc., 2008. Tüm hakları Saklıdır
PROV-011
Son Güncelleme: 03/08
Provigil (modafinil) hasta bilgi sayfası (Sade ingilizce)
Hakkında detaylı bilgi Uyku Bozukluklarında Belirtiler, Belirtiler, Nedenleri, Tedavileri
Bu monograftaki bilgilerin olası tüm kullanımları, talimatları, önlemleri, ilaç etkileşimlerini veya yan etkileri kapsaması amaçlanmamıştır. Bu bilgiler genelleştirilmiştir ve özel tıbbi tavsiye olarak tasarlanmamıştır. Aldığınız ilaçlar hakkında sorularınız varsa veya daha fazla bilgi edinmek istiyorsanız, doktorunuza, eczacınıza veya hemşirenize danışın.
geri dön:
~ uyku bozuklukları ile ilgili tüm makaleler



